Technical Note : ข้อมูลทางเทคนิค
Gel electrophoresis of protein
Life Science
การแยกโปรตีนโดยวิธีอิเลคโตรโฟรีซีสสามารถนำไปประยุกต์ใช้ได้ในงานต่างๆ เช่น...
การแยกโปรตีนโดยวิธีเจลอิเลคโตรโฟรีซีส (Gel electrophoresis of protein)
การแยกโปรตีนโดยวิธีอิเลคโตรโฟรีซีสสามารถนำไปประยุกต์ใช้ได้ในงานต่างๆ เช่น การเปรียบเทียบและการวิเคราะห์รูปแบบ (pattern) ของสารตัวอย่างโปรตีนจากเนื้อเยื่อหรือเซลล์ที่มาจากแหล่งต่างๆ การตรวจสอบความผิดปกติของโปรตีนที่อาจเกิดจาการผ่าเหล่า (mutation) การแยกและทำให้บริสุทธิ์ การทดสอบคุณสมบัติของโปรตีนทางอิมมูโนวิทยา และการตรวจหาขนาดของโปรตีน (molecular weight) เจลพอลิอะคริลาไมด์เกิดจากปฏิกิริยาการเชื่อมต่อกันของหน่วยเดี่ยวของอะคริลาไมด์ (acrylamide monomer) จนได้เป็นสายโซ่ยาวและเชื่อมกันเป็นโครงข่ายด้วยพันธะโคเวเลนต์ (covalent bond) ซึ่งมีหมู่ฟังก์ชัน 2 หมู่ (bi-functional compound) เช่น N,N'-เมทิลีน บิสอะคริลาไมด์ (N,N'-methylene bisacrylamide ย่อว่า บิสอะคริลาไมด์) ปฏิกิริยาดังกล่าวทำให้ได้โครงสร้างที่มีลักษณะเป็นรูพรุน ซึ่งมีขนาดแตกต่างกันตามขนาดโมเลกุลของโปรตีนที่ต้องการแยก ดังนั้นระหว่างการแยกด้วยบนเจลพอลิอะคริลาไมด์ด้วยกระแสไฟฟ้า โมเลกุลโปรตีนจะถูกคัดกรองด้วยตะแกรงสามมิติ (sieving effect) จึงทำให้โมเลกุลขนาดใหญ่เคลื่อนที่ช้ากว่าโปรตีนขนาดเล็ก และการแยกโปรตีนที่ทำงานได้ตามธรรมชาติ (native protein) ด้วยกระแสไฟฟ้าบนเจลพอลิอะคริลาไมด์ในสารละลายบัฟเฟอร์ที่ไม่ทำให้โปรตีนเสียสภาพ (non-dissociating buffer หรือ non-denaturing buffer) เช่น ทริสคลอไรด์ (Tris-HCl) นั้น ขึ้นอยู่กับความหนาแน่นของประจุและขนาดของโปรตีนความสามารถในการคัดกรองของการแยกด้วยวิธีนี้ขึ้นอยู่กับว่า ขนาดของรูพรุนของเจลมีค่าใกล้เคียงกับขนาดของโปรตีนที่เคลื่อนที่ไปบนเจลมากน้อยเพียงใด รูพรุนของเจลพอลิอะคริลาไมด์จะแปรผกผันกับความเข้มข้นของอะคริลาไมด์ในของผสมเจล (หากความเข้มข้นของอะคริลาไมด์เพิ่มขึ้น ขนาดของรูพรุนจะเล็กลง) และสัดส่วนของตัวเชื่อมโครงข่ายบิสอะคริลาไมด์ที่ใช้ด้วย ในทางปฏิบัติ สัดส่วนของตัวเชื่อมโครงข่ายจะมีค่าคงที่และประสิทธิภาพของรูพรุนจะเปลี่ยนแปลงไปตามการเลือกใช้ความเข้มข้นของหน่วยเดี่ยว ๆ ของอะคริลาไมด์ การแยกโปรตีนส่วนใหญ่ใช้เจลที่มีความเข้มข้นของอะคริลาไมด์อยู่ในช่วงร้อยละ 5 - 15 ซึ่งเจลที่มีร้อยละของอะคริลาไมด์ต่ำจะให้ขนาดรูพรุนใหญ่ที่สุดซึ่งเหมาะสำหรับแยกโปรตีนที่มีขนาดใหญ่ให้เป็นแถบด้วยกระแสไฟฟ้า และการเพิ่มความเข้มข้นของอะคริลาไมด์จะช่วยแยกโปรตีนที่มีขนาดเล็กได้ดีขึ้น
หลักการทั่วไปของการแยกโปรตีนโดยเจลอิเลคโตรโพรีซีสคือ โปรตีนที่มีประจุจะถูกบังคับให้เคลื่อนที่ในสนามไฟฟ้าไปยังขั้วไฟฟ้าที่มีประจุตรงข้าม การเคลื่อนที่นี้จะถูกต้านโดยปฏิกิริยาระหว่างสารกับร่างแหเจล ซึ่งทำหน้าที่เป็น molecular sieve ดังนั้นการเคลื่อนที่ของโปรตีนจึงขึ้นอยู่กับขนาด รูปร่าง และปรุจุสุทธิของโปรตีน การแยกโปรตีนด้วยโพลีอะคริลลาไมด์มี 2 ระบบคือ
1. ระบบที่ไม่ทำให้โปรตีนเสียสภาพ (non-denaturing gel หรือ native gel electrophoresis) วิธีโปรตีนอยู่อยู่ในสภาพธรรมชาติ ซึ่งสามารถนำโปรตีนที่แยกได้นี้ไปตรวจสอบหาแอคติวิตีได้ แต่ไม่สามารถแยกความแตกต่างของรูปร่าง ขนาด หรือประจุของโปรตีนได้ คือ โปรตีนที่มีน้ำหนักโมเลกุลต่างกันอาจเคลื่อนที่ได้เท่ากันในระบบนี้ ดังนั้นระบบนี้จึงเหมาะสำหรับใช้แยกหรือจำแนกโปรตีนชนิดต่างๆออกจากกันแต่ไม่เหมาะสำหรับใช้ตรวจหรือยืนยันความบริสุทธิ์ หรือหาน้ำหนักโมเลกุลของโปรตีน
2. ระบที่ทำให้โปรตีนเสียสภาพ (denature systems โปรตีนที่แยกได้ไม่สามารถนำมาทดสอบหาแอคติวิตีได้ แต่สามารถบอกขนาดน้ำหนักโมเลกุลของโปรตีนต่างกันได้ ระบบน้ำจึงนำมาใช้ตรวจสอบความบริสุทธิ์และขนาดของโปรตีน รวมทั้งสามารถนำไปตรวจหาคุณสมบัติของโปรตีนทางอิมมูโนวิทยา โดยวิธีการทำ western blot การแยกโปรตีนในระบบนี้ได้แก่ วิธี SDS-PAGE ซึ่ง SDS เป็นสาร detergent ทำให้โปรตีนเสียสภาพ นอกจากนี้ยังมีสาร acid-urea, triton-acid-urea เป็นต้น
การทำอิเลคโตรโฟรีซีสมีทั้งแบบ one-dimension และ two-dimension ซึ่งในที่นี้จะขอกล่าวถึงการทำ 2 dimension gel
อิเลคโตรโฟรีซีสในการแยกโปรตีนใน 2 มิติ (2 dimension gel electrophoresis)
เป็นเทคนิคในการแยกโปรตีนโดยการรวม IEF และ SDS-PAGE เข้าด้วยกัน โดยมิติแรกโปรตีนจะถูกแยกด้วย IEF ซึ่งจะแยกโดยอาศัยความต่างของ pI จากนั้นจึงแยกโปรตีนอีกครั้งในมิติที่สองด้วยวิธี SDS-PAGE ซึ่งอาศัยความแตกต่างของน้ำหนักโมเลกุล
1. Isoelectric Focusing (IEF)
การแยกโดยเน้นประจุเป็นกลางในสนามไฟฟ้า (IEF) ซึ่งโดยทั่วไปเรียกว่า อิเล็กโทรโฟกัสซิ่ง (electrofocusing) เป็นวิธีการแยกโมเลกุลที่มีประจุแตกต่างกัน สำหรับการแยกโปรตีนด้วยวิธีนี้ ของผสมโปรตีนต้องอยู่ภายใต้สนามไฟฟ้าโดยใช้ตัวค้ำจุนที่ไม่เกิดปฏิกิริยาได้ง่าย (inert support) โดยการแปรผันความแตกต่างของค่า pH ทำให้บริเวณขั้วบวก (anode) มีค่า pH ต่ำกว่าบริเวณขั้วลบ (cathode) และช่วงค่าความเป็นกรด-เบสที่เลือกใช้ต้องรวมถึงค่า pH ที่โปรตีนมีประจุสุทธิเป็นศูนย์ (isoelectric point, pI) ของโปรตีนที่เราสนใจด้วย โปรตีนที่มีค่า pH ต่ำกว่าค่า pI จะมีประจุเป็นบวกและเคลื่อนที่เข้าหาขั้วลบ เมื่อโปรตีนเคลื่อนที่ไปจะทำให้ค่า pH ลดลงจนกระทั่งค่า pH เท่ากับค่า pI ทำให้มีประจุสุทธิเป็นศูนย์ (หรือไม่มีประจุนั่นเอง) และโปรตีนจะหยุดเคลื่อนที่ ในทางกลับกัน เมื่อโปรตีนมีค่า pH สูงกว่าค่า pI โปรตีนจะมีประจุเป็นลบและเคลื่อนเข้าหาขั้วบวก ดังนั้นโปรตีนแต่ละชนิดจึงเคลื่อนเป็นแถบเข้าขั้วไฟฟ้าและไปหยุดที่ค่า pH เท่ากับค่า pI
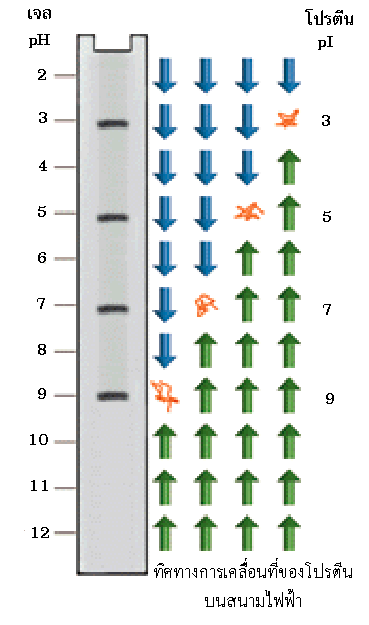
ภาพที่ 1 แสดงการเคลื่อนที่ของโปรตีนภายใต้สนามไฟฟ้า เมื่อค่า pH เท่ากับค่า pI โปรตีนจะมีประจุสุทธิเป็นศูนย์และหยุดเคลื่อนที่ เห็นเป็นแถบปรากฏอยู่บนเจล
การแปรผันค่า pH อย่างคงที่ระหว่างขั้วไฟฟ้าเกิดขึ้นโดยเติมของผสมของแอมโฟไลต์ตัวพา (carrier ampholyte) ซึ่งมีน้ำหนักโมเลกุลน้อยในตัวค้ำจุน แอมโฟไลต์ตัวพาเป็นสารที่มีสมบัติเป็นได้ทั้งกรดและเบสขึ้นกับสภาพของ pH และชนิดที่มีผลิตขายเชิงการค้าเป็นสารพวกกรดพอลิอะมิโนพอลิคาร์บอกซิลิกสายโซ่ตรงชนิดสังเคราะห์ (aliphatic polyamino-polycarboxylic acid) ซึ่งต้องเลือกช่วง pH ให้เหมาะสมกับแต่ละค่า pI ของสารนี้ แอมโฟไลต์ตัวพามีทั้งในช่วง pH กว้าง (เช่น pH 3 - 10) และช่วง pH แคบ (เช่น pH 7 – 8 การแยกด้วยวิธี IEF นี้ขึ้นอยู่กับธรรมชาติของตัวค้ำจุนที่ใช้ การแยกโปรตีนจำนวนมากโดยวิธี IEF ทำได้โดยบรรจุแอมโฟไลต์ตัวพาในสารละลายซูโครสที่แปรผันความหนาแน่นลงในคอลัมน์แก้ว สารละลายซูโครสที่มีความหนืดนี้จะทำหน้าที่เป็นตัวค้ำจุนให้โปรตีนเคลื่อนที่ได้ช้าลงและไม่เกิดการผสมของสารเนื่องจากการพา (convective mixing) จากนั้นต่อขั้วไฟฟ้าด้านบน (ขั้วบวก) เข้ากับภาชนะบรรจุกรด (เช่น กรดฟอสฟอริก) และต่อขั้วไฟฟ้าด้านล่างเข้ากับภาชนะบรรจุด่าง (เช่น NaOH) เพื่อให้มีค่าความเป็นกรด-เบสแตกต่างกันในคอลัมน์ระหว่างการแยกด้วยกระแสไฟฟ้า เมื่อเตรียมคอลัมน์เสร็จใส่ตัวอย่างลงในคอลัมน์ และการแยกจะดำเนินไปจนกระทั่งถึงค่า pI ของโปรตีนนั้น ๆ เก็บแถบโปรตีนแต่ละชนิดโดยผ่านท่อด้านล่างและเก็บชั้นส่วน (fraction) ของตัวอย่างแยกจากกัน วิธีนี้ไม่นิยมนำมาใช้ในการเตรียมโปรตีนเนื่องจากแอมโฟไลต์ตัวพามีราคาแพง สำหรับงานที่ต้องการโปรตีนที่มีความบริสุทธิ์สูงและใช้ปริมาณของโปรตีนน้อย (ในหน่วยมิลลิกรัมของโปรตีน) สามารถเตรียมได้โดยใช้แผ่นเจล เช่น เซฟาเดกซ์ (Sephadex) และแยกด้วยกระแสไฟฟ้าตามแนวนอนในภาชนะที่หล่อด้วยน้ำเย็น หลังจากการแยกด้วยกระแสไฟฟ้าแล้ว หั่นส่วนของเจลซึ่งมีโปรตีนที่เราสนใจออกทีละชิ้น ใส่ลงในหลอดทดลอง และชะโปรตีนออกจากเจลด้วยสารละลายบัฟเฟอร์
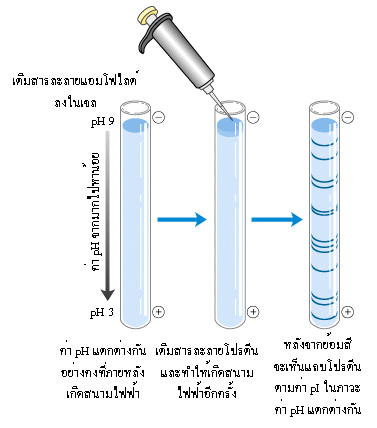
ภาพที่ 2 การทำโปรตีนให้บริสุทธิ์ด้วยวิธี IEF เริ่มจากเตรียมคอลัมน์บรรจุด้วยสารละลายแอมไฟไลต์ จากนั้นต่อขั้วไฟฟ้าเพื่อให้การแปรผันค่า pH จากนั้นใส่ของผสมโปรตีนลงในคอลัมน์และให้กระแสไฟฟ้าอีกครั้ง รอประมาณ 2 - 3 ชั่วโมงเพื่อให้โปรตีนเคลื่อนที่ไปหยุดที่ค่า pI ของตัวเอง ภายหลังจาย้อมสีจะเห็นโปรตีนแยกออกเป็นแถบ
การแยกด้วยวิธี IEF บนแผ่นเจลตามแนวนอนนิยมใช้ทั่วไปในปัจจุบัน โดยใช้แผ่นเจลพอลิอะคริลาไมด์บาง ๆ หรือแผ่นเจลอะกาโรสที่ผนึกติดไว้บนแผ่นกระจกหรือแผ่นพลาสติก และแช่อยู่ในสารละลายแอมโฟไลต์ตัวพาในช่วง pH ที่ถูกต้อง แผ่นเจลนี้สามารถเลือกซื้อได้จากบริษัทต่าง ๆ หรือเตรียมได้เองในห้องปฏิบัติการ แต่สิ่งที่สำคัญคือ ต้องระวังในการเลือกใช้ชนิดและความเข้มข้นของเจล เพราะหากเลือกไม่ถูกต้องการแยกด้วยวิธีนี้จะไม่เกิดบนพื้นฐานของการแยกตามความแตกต่างของประจุเพียงอย่างเดียว แต่จะมีการคัดเลือกตามขนาดโมเลกุลมาร่วมด้วย ด้วยเหตุนี้จึงต้องเลือกใช้แผ่นอะกาโรสซึ่งมีรูพรุนใหญ่กว่าแผ่นเจลพอลิอะคริลาไมด์ ทำให้สามารถแยกโปรตีนที่มีโมเลกุลขนาดใหญ่กว่าแผ่นเจลพอลิอะคริลาไมด์ หากเลือกใช้แผ่นเจลพอลิอะคริลาไมด์ต้องเลือกความเข้มข้นของเจลที่ให้รูพรุนขนาดใหญ่เพื่อลดการคัดกรองด้วยขนาดโมเลกุล แผ่นเจลที่เตรียมได้ส่วนใหญ่มีความหนาประมาณ 1 - 2 มิลลิเมตร แต่แผ่นเจลที่มีขายกันทั่วไปจะมีความบางมาก (ultra-thin gel) ซึ่งหนาประมาณ 0.1 - 0.25 มิลลิเมตร เพื่อทำให้มีราคาถูกลง (โดยลดปริมาณแอมโฟไลต์ซึ่งมีราคาแพง) ใช้เวลาในการแยกด้วยกระแสไฟฟ้าน้อยลง (เนื่องจากสามารถใช้ความต่างศักย์ไฟฟ้าสูงได้) และมีความสามารถในการแยกสูงเจลบนแผ่นกระจกหรือแผ่นพลาสติกตามแนวนอนต้องวางอยู่ในภาชนะหล่อน้ำเย็น เพื่อให้ความร้อนในการแยกด้วยกระแสไฟฟ้ากระจายตัวอย่างทั่วถึงและไม่ทำลายแถบโปรตีนที่แยกออกจากกัน การวิเคราะห์ตัวอย่างแบบนี้ใช้ปริมาณเพียงไม่กี่ไมโครกรัมเท่านั้น วิธีที่ง่ายที่สุดเพื่อใส่ตัวอย่างลงบนเจล คือ จุ่มชิ้นกระดาษกรองลงในสารละลายตัวอย่าง จากนั้นเสียบแผ่นกระดาษเข้าไปในเจลที่จุดเริ่มต้น ภายหลังการแยกด้วยกระแสไฟฟ้าไประยะเวลาสั้น ๆ เพื่อให้โปรตีนเคลื่อนผ่านเข้าไปในเจล จึงดึงกระดาษกรองออก และปล่อยให้การแยกด้วยกระแสไฟฟ้าดำเนินไปภายในระยะเวลา 2 - 3 ชั่วโมง เพื่อให้โปรตีนเคลื่อนที่ไปถึงจุด pI เมื่อนำแผ่นเจลไปย้อมสีจะเห็นแถบโปรตีนปรากฏขึ้นในตำแหน่งค่า pI ของตัวเอง หากต้องการแยกโปรตีนหลาย ๆ ตัวอย่างบนแผ่นเจลก็ทำได้โดยใช้กระดาษกรองหลาย ๆ ชิ้น จุ่มกระดาษกรองแต่ละชิ้นลงในตัวอย่างที่ต่างกัน และนำไปเสียบในแผ่นเจลเรียงต่อกันไปเรื่อย ๆ
การแยกด้วยกระแสไฟฟ้าบนเจลพอลิอะคริลาไมด์ที่มี SDS เป็นส่วนประกอบ (SDS-PAGE)
เป็นวิธีที่ใช้ตรวจสอบความบริสุทธิ์ของโปรตีนระหว่างขั้นตอนการทำโปรตีนให้บริสุทธิ์ นอกจากนี้ยังเป็นวิธีที่ใช้ในการศึกษาและหาน้ำหนักโมเลกุลของโปรตีนหรือหน่วยย่อย (subunit) ของโปรตีน เมื่อใช้คู่กับเทคนิคทาง gel filtration chromatography ก็จะทำให้ทราบว่าโปรตีนนั้นๆประกอบด้วยหน่วยย่อยกี่หน่วย หลักการของ SDS-PAGE คือ SDS ซึ่งเป็น detergent ที่มีประจุลบไปเกาะกับโปรตีนอย่างแน่นหนามากทำให้โปรตีนทั้งหมดมีประจุลบ นอกจากนี้ SDS ยังทำให้โปรตีนเสียสภาพ เปลี่ยนสภาพจากทรงกลม (globular) ไปอยู่ในสภาพที่เหยียดตรง โปรตีนที่ประกอบด้วยหน่วยหลายหน่วยเกาะกันอยู่ก็จะแยกออกเป็นแต่ละหน่วยย่อย ดังนั้นการเคลื่อนที่ในสนามไฟฟ้าของโปรตีนทุกตัวในกรณีนี้ จึงเป็นการเคลื่อนที่โดยอาศัยความแตกต่างในน้ำหนักโมเลกุลเพียงอย่างเดียว โดยจะเป็นการเคลื่อนที่ไปสู่ขั้วไฟฟ้าบวกในอัตราส่วนผกผันกับค่า log ของน้ำหนักโมเลกุล ซึ่งหมายความวย่าจะสายมารถหาน้ำหนักโมเลกุลของโปรตีนได้ จากระยะการเคลื่อนที่ของโปรตีนที่ต้องการทราบน้ำหนักโมเลกุลกับโปรตีนมาตรฐานที่ทราบน้ำหนักโมเลกุลแล้ว นอกจากนี้การปรากฏของแถบโปรตีนเพียงแถบเดี่ยใน SDS-PAGE ยังเป็นตัวบ่งชี้ถึงความบริสุทธิ์ของโปรตีน
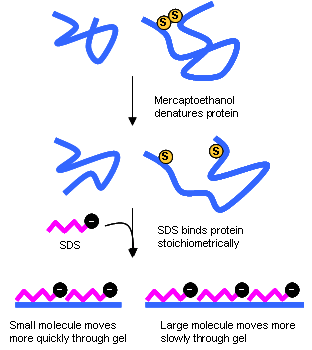
ภาพที่ 3 แสดงการเข้าจับของ SDS กับโปรตีน ซึ่งจะทำให้โปรตีนมีรูปร่างเป็นเส้นเหยียดและมีประจุลบ
วิธีการทำ SDS-PAGE มีความแตกต่างกันบ้างในแต่ละวิธี เช่น วิธีของ Weber และ Osborne เป็นแบบ continuous polyacrylamide gel electrophoresis ใช้ phosphate buffer ส่วนวิธีของ Laemmmli ซึ่งเป็นวิธีที่นิยมใช้กันมากและทำในรูปของ slab gel เป็นแบบ discontinuous polyacrylamide gel electrophoresis ใช้ 0.5 M Tris-HCl, pH6.8 สำหรับ concentrate stacking gel buffer, 1.5 M Tris-HCl, pH 8.8 สำหรับ concentrated resolving gel buffer หรือ concentrated separating gel buffer และ 0.025 M Tris, 0.192 M Glycine, 0.1% w/v SDS, pH8.3 สำหรับ electrode buffer วิธีของ discontinuous gel electrophoresis เป็นวิธีที่ gel buffer และ electrode buffer จะเกิดการรวมตัวกันและช่วยในการทำให้ตัวอย่างที่แยกในระหว่างการเคลื่อนที่ในกระแสไฟฟ้าราวมตัวอัดแน่นและเข้มข้น นอกจากนี้ stacking gel ที่ %T ต่ำจะช่วยในการรวมตัวอัดแน่นกันของตัวอย่าง ส่วน separating gel สามารถที่จะเปลี่ยนแปลงค่า %T ตามความต้องการขึ้นอยู่กับการแยกขนาดของโปรตีน และยังสามารถใช้แบบ gradient ได้จาก %T ต่ำ (ด้านบน) ไปสู่ %T สูง (ด้านล่าง) ของเจลได้ เพื่อให้การแยกตัวอย่างที่มีความแตกต่างของขนาดได้ดียิ่งขึ้น
.jpg)
ภาพที่ 4 แสดงการวิเคราะห์โปรตีนด้วยวิธี SDS-PAGE แบบ discontinuous gel
สำหรับการวิเคราะห์ด้วย SDS-PAGE นั้น ของผสมโปรตีนจะถูกทำให้เสียสภาพโดยความร้อนที่อุณหภูมิ 100°ซ เป็นเวลา 2 - 5 นาทีในสารละลายที่มี SDS มากเกินพอและมีสารประเภทไทออล (thiol) เป็นองค์ประกอบ เช่น 2-เมอร์แคปโทเอทานอล (2-mercaptoethanol) เพื่อทำลายพันธะไดซัลไฟด์ (disulphide bond) ในโปรตีน ภายใต้ภาวะดังกล่าวนี้โปรตีนส่วนใหญ่จะเกาะกับ SDS ในอัตราส่วนโดยน้ำหนักที่คงที่ (1.4 กรัมของ SDS ต่อพอลิเพปไทด์ 1 กรัม) จากนั้นนำของผสมโปรตีนแต่ละตัวอย่างใส่ลงบนเจลทรงกระบอกแต่ละแท่งหรือแต่ละช่องบนเจลแผ่น และนำไปแยกด้วยกระแสไฟฟ้า ซึ่งทั้งเจลและบัฟเฟอร์ที่ใช้ในการแยกมี SDS เป็นองค์ประกอบอยู่ โปรตีนเทียบเคียงจะให้ผลในลักษณะเดียวกับเจลช่องอื่น ๆ โดยโปรตีนจะเคลื่อนที่ไปตามน้ำหนักโมเลกุลของตัวเอง ภายหลังจากการแยกด้วยกระแสไฟฟ้า ตำแหน่งของแถบโปรตีนที่แยกออกจากกันจะปรากฏขึ้นเมื่อย้อมด้วยสี เช่น สีคูแมซีบลู (Coomassie Blue) หรือสีสารประกอบของเงิน (silver stain) นการแยกด้วยวิธี SDS-PAGE SDS จะจับโปรตีนในอัตราส่วนโดยน้ำหนักหนักที่คงที่ตลอดทั้งเจล (กล่าวคือ โปรตีนที่มีขนาดใหญ่มี SDS เกาะอยู่มาก) ทำให้โปรตีนทุกชนิดมีค่าความหนาแน่นของประจุต่อน้ำหนักโปรตีนเท่ากัน การแยกโปรตีนด้วยวิธีนี้จึงอาศัยการแยกโดยขนาดเพียงอย่างเดียว โดยไม่มีจำนวนประจุมาเกี่ยวข้อง และเนื่องจากระยะทางที่เคลื่อนที่ไปของสายพอลิเพปไทด์บนเจลมีความสัมพันธ์โดยตรงกับขนาดของพอลิเพปไทด์เท่านั้น การแยกโปรตีนที่เราสนใจบนเจลนี้ทำได้โดยเทียบน้ำหนักโมเลกุลระหว่างโปรตีนตัวอย่างกับโปรตีนเทียบเคียง ในกรณีที่เรามั่นใจว่า น้ำหนักของโปรตีนที่เราต้องการแตกต่างจากโปรตีนอื่น ๆ อย่างชัดเจน เราสามารถแยกโปรตีนบนเจลเพื่อนำไปศึกษาองค์ประกอบได้ (โดยที่ไม่ต้องเทียบกับโปรตีนเทียบเคียงที่ทราบน้ำหนักโมเลกุลแล้ว)
การแยกบนเจลด้วยกระแสไฟฟ้าสองมิติ (two-dimensional gel electrophoresis: 2D gel)
การแยกพอลิเพปไทด์บนเจลด้วยกระแสไฟฟ้าในทิศทางเดียว หรือที่เรียกว่า การแยกด้วยกระแสไฟฟ้ามิติเดียว (one-dimensional electrophoresis) เป็นการแยกตามขนาดและประจุร่วมกันบนเจลในภาวะที่โปรตีนที่ถูกทำให้เสียสภาพไป หากโปรตีนถูกทำให้เสียสภาพ การแยกมิติเดียวจะเป็นการแยกตามขนาด (SDS-PAGE) หรือแยกตามประจุ (isoelectric focusing, IEF) อย่างใดอย่างหนึ่งเท่านั้น สำหรับการแยกด้วยกระแสไฟฟ้ามิติเดียวนี้ พอลิเพปไทด์ตั้งแต่ 2 ชนิดขึ้นไปมีโอกาสเคลื่อนที่ไปพร้อม ๆ กันและไปหยุดที่ตำแหน่งที่ใกล้เคียงกันมาก จึงเห็นเป็นแถบเดียว โดยเฉพาอย่างยิ่งในกรณีตัวอย่างตั้งต้นเป็นของผสมโปรตีนซับซ้อน การเคลื่อนที่ของโปรตีนหลายชนิดไปพร้อม ๆ กันจะบอกถึงความซับซ้อนของของผสมโปรตีน ซึ่งอาจทำให้สรุปผลความบริสุทธิ์ของตัวอย่างผิดพลาดไปได้
สำหรับการแยกบนเจลด้วยกระแสไฟฟ้าไปในสองทิศทางที่ตั้งฉากกันและในแต่ละทิศทางอาศัยหลักการแยกที่ต่างกัน เรียกว่า การแยกด้วยกระแสไฟฟ้าสองมิติ (two-dimensional electrophoresis) อาจทำได้โดยแยกโปรตีนตามประจุในมิติแรกและติดตามด้วยการแยกตามขนาดในมิติที่สอง การแยกในมิติแรกตามประจุเป็นการแยกตัวอย่างโปรตีนด้วยกระแสไฟฟ้าในเจล แท่งพอลิอะคริลาไมด์ ซึ่งปกติแยกโดยอาศัยวิธี IEF จากนั้นนำเจลแท่งที่ผ่านการแยกด้วยกระแสไฟฟ้าในมิติแรกแล้วมาวางในแนวนอนต่อกับขอบบนของแผ่นเจลที่เตรียมไว้สำหรับแยกในมิติที่สองด้วยวิธี SDS-PAGE สายพอลิเพปไทด์ที่แยกตามประจุในเจลแท่ง (ในมิติแรก) จะเคลื่อนที่เข้าไปในแผ่นเจลและแยกตามขนาดของสายพอลิเพปไทด์ การแยกในมิติที่ 2 นี้อาจใช้แผ่นเจลพอลิอะคริลาไมด์ที่มีความเข้มข้นเดียวกันตลอดทั้งเจล หรือใช้แผ่นเจลที่มีความเข้มข้นแตกต่างกัน เมื่อแยกด้วยวิธี SDS-PAGE ในมิติที่สองเรียบร้อยแล้ว โปรตีนจะแยกออกจากกันและปรากฏเป็นจุด (เมื่อนำมาย้อมด้วยสี) หากวัดค่า pH ที่แตกต่างกันในแท่งเจลในมิติแรกและเปรียบเทียบกับสายพอลิเพปไทด์ที่ทราบน้ำหนักโมเลกุลเมื่อแยกด้วยวิธี SDS-PAGE ในมิติที่สอง จะสามารถประมาณค่า pH ที่มีประจุสุทธิเป็นศูนย์ (pI) และน้ำหนักโมเลกุลของสายพอลิเพปไทด์ที่เราสนใจได้ง่ายโดยพิจารณาจากตำแหน่งตามแนวนอนและแนวตั้ง ตามลำดับ
หลักการทำ 2-D PAGE มีขั้นตอนคร่าวๆตาลำดับดังนี้
1. แยกโปรตีนด้วย isoelectric focusing ใน tube gel หรือ rod gel ที่มีเส้นผ่าศูนย์กลางประมาณ 1-3 มิลลิเมตร หรือซื้อเจลที่เตรียมเรียบร้อยแล้วอยู่บนแผ่นฟิล์ม เช่น IPG strip
2. นำ IEF เจลมาเอา ampholytes ออก โดยการเปลี่ยนบัฟเฟอร์ใน IEF gel เป็น SDS buffer
3. นำเจลที่แยกด้วย IEF ในมิติที่หนึ่ง มาวางให้แนบกับหน้าเจลของ SDS-PAGE ตามแนวนอน ในบางกรณีที่โปรตีนที่ต้องการแยกเป็น basic proteins ซึ่งอาจแยกไม่ได้ดีใน IEF ก็อาจใช้วิธี non-equilibrium isoelectric focusing หรือมักเรียกว่า non-equilibrium pH gradient electrophoresis (NEPHGE)
4. นำไปแยกโปรตีนในมิติที่สองด้วยวิธี SDS-PAGE
5. ย้อมโปรตีนที่ถูกแยกได้
6. วิเคราะห์รูปแบบ (pattern) ของโปรตีนที่ได้ อาจใช้โปรแกรมคอมพิวเตอร์และฐานข้อมูล 2-D spot มาช่วยวิเคราะห์

ภาพที่ 5 แสดงการวิเคราะห์โปรตีนแบบ 2D-gel
เนื่องจากการแยกด้วยกระแสไฟฟ้าสองมิติบนเจลพอลิอะคริลาไมด์เป็นการแยกที่รวม 2 ขั้นตอนเข้าด้วยกัน จึงเป็นวิธีที่แยกที่มีความสามารถสูงสุดในบรรดาการแยกโปรตีนด้วยกระแสไฟฟ้าทั้งหมดที่มีใช้อยู่กันในปัจจุบัน สำหรับวิธี SDS-PAGE หรือ IEF นั้นเหมาะสมสำหรับการวิเคราะห์ตัวอย่างโปรตีนในบางขั้นตอนของแผนการทำโปรตีนให้บริสุทธิ์เท่านั้น และการแยกบนเจลด้วยกระแสไฟฟ้าสองมิติควรนำมาใช้ตรวจสอบความบริสุทธิ์ของโปรตีนที่เราสนใจในขั้นตอนสุดท้ายว่า มีความบริสุทธิ์มากน้อยเพียงใด อย่างไรก็ตาม ไม่สามารถยืนยันได้ว่าจุดเดี่ยว ๆ ที่ได้จากการแยกบนเจลด้วยกระแสไฟฟ้าสองมิติ คือ สายพอลิเพปไทด์ชนิดเดียว การแยกบนเจลด้วยกระแสไฟฟ้าสองมิตินี้เป็นการลดโอกาสที่สายพอลิเพปไทด์ตั้งแต่ 2 ชนิดขึ้นไปซึ่งมีประจุและขนาดต่างกันจะเคลื่อนที่มาอยู่ในตำแหน่งเดียวกัน ในกรณีที่พอลิเพปไทด์ตั้งแต่ 2 ชนิดขึ้นไปอาจเคลื่อนที่มาเป็นกลุ่ม ไม่ใช่เคลื่อนที่มาเป็นสายเดี่ยว ๆ เช่น โปรตีนที่แยกจากเยื่อหุ้มต่าง ๆ อาจเกาะกลุ่มกันเป็นโครงสร้างที่มีความเสถียรและไม่สามารถแยกออกจากกันได้เมื่อใช้การแยกแบบ IEF และ SDS-PAGE ในกรณีเช่นนี้จำเป็นต้องใส่สารเคมีอื่นบางชนิดในการเตรียมตัวอย่างและแยกด้วยกระแสไฟฟ้า เช่น ยูเรีย กวานิดีนไฮโดรคลอไรด์ (guanidine hydrochloride) เพื่อทำให้โปรตีนแยกตัวออกจากกันโดยสมบูรณ์
Relate product
Product catalog number
ZOOM® IEF Fractionator combo kit ZF10001
ZOOM® IEF Fractionator ZF10002
ZOOM® Basic protein kit ZF10006
ZOOM® Disk pH 3.0 ZD10030
ZOOM® Disk pH4.6 ZD 10046
ZOOM® Disk pH 5.4 ZD 10054
ZOOM® Disk pH6.2 ZD 10062
ZOOM® Disk pH7.0 ZD 10070
ZOOM® Disk pH9.1 ZD 10091
ZOOM® Disk pH10.0 ZD 10010
ZOOM® Disk pH 12.0 ZD10012
ZOOM® Urea ZU10001
ZOOM® Thiourea ZU10002
ZOOM® Carrier Ampholytes pH3-10 ZM0021
Novex IEF Anode Buffer LC5300
Novex IEF Cathode Buffer LC5310
ZOOM® Focusing buffer pH3-7 ZB10037
ZOOM® Strips pH3-10L ZM0018
ZOOM®IPG Runner Combo kit ZM0002
More info: www.invitrogen.com














